Kwasy Karboksylowe Sprawdzian Chemia Nowej Ery 3
Kwasy Karboksylowe: Twój Przyjaciel w Świecie Chemii
Hej! Przygotowujesz się do sprawdzianu z chemii, a kwasy karboksylowe spędzają Ci sen z powiek? Spokojnie, zaraz je oswoimy! Pomyśl o nich jak o składnikach, które znasz z życia codziennego, tylko teraz spojrzymy na nie przez mikroskop.
Co to w ogóle są kwasy karboksylowe? Wyobraź sobie węglowodór, czyli łańcuch atomów węgla i wodoru. Do tego łańcucha doklejmy grupę karboksylową (–COOH). I voila! Mamy kwas karboksylowy. To ta grupa –COOH nadaje im charakterystyczne właściwości.
Budowa i Wzory: Wizualna Pomoc
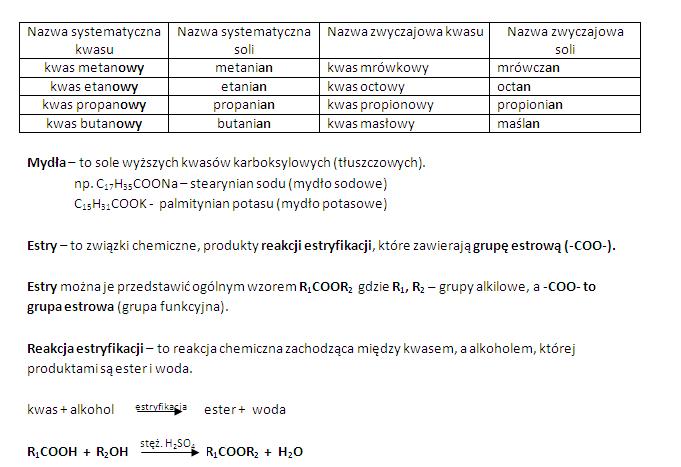
Spójrzmy na to bardziej obrazowo. Kwas metanowy (kwas mrówkowy) ma najprostszą budowę: H-COOH. Kwas etanowy (kwas octowy), który znasz z octu, wygląda tak: CH3-COOH. Widzisz? Grupa karboksylowa (–COOH) jest zawsze na końcu łańcucha. To jak wagonik doczepiony do pociągu!
Must Read
Wzory strukturalne pokazują, jak atomy są połączone. W kwasie mrówkowym, atom węgla jest połączony z atomem wodoru i grupą karboksylową. W kwasie octowym, atom węgla łączy się z trzema atomami wodoru i grupą karboksylową. Spróbuj narysować to sam, żeby lepiej zapamiętać!
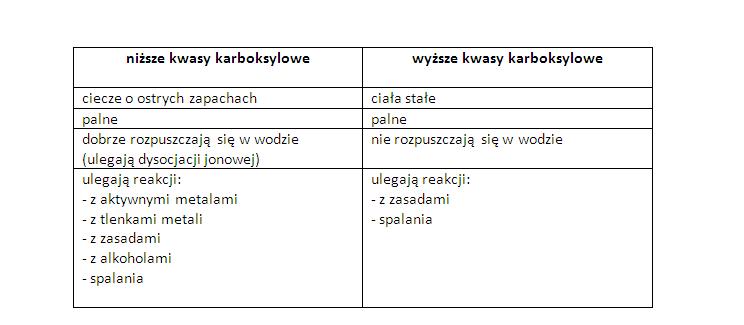
Właściwości: Co je Wyróżnia?
Kwasy karboksylowe mają pewne cechy, które je charakteryzują. Są polarne, co oznacza, że mają na jednym końcu ładunek dodatni, a na drugim ujemny. To sprawia, że dobrze rozpuszczają się w wodzie, zwłaszcza te o krótkich łańcuchach.
Kolejna ważna cecha to kwasowość. Oddają protony (H+), stąd nazwa "kwas". Kwas octowy, który dodajesz do sałatki, nadaje jej kwaśny smak właśnie dlatego. Pamiętaj jednak, że nie wszystkie kwasy karboksylowe są tak samo mocne. Niektóre oddają protony łatwiej, inne trudniej.
Reakcje: Co z Nimi Można Zrobić?
Kwasy karboksylowe lubią reagować! Jedną z najważniejszych reakcji jest estryfikacja. Reagują z alkoholami, tworząc estry i wodę. Estry to związki o przyjemnym zapachu, często wykorzystywane w przemyśle spożywczym i perfumeryjnym. Wyobraź sobie zapach jabłek – to zasługa estrów!
Inną ważną reakcją jest neutralizacja. Kwasy karboksylowe reagują z zasadami, tworząc sole i wodę. To podobna reakcja do tej, którą znasz z kwasów nieorganicznych, np. kwasu solnego. Pamiętaj, że sól to nie tylko ta kuchenna! To ogólna nazwa związku powstałego w reakcji kwasu i zasady.
Przykłady i Zastosowania: Gdzie je Znajdziemy?
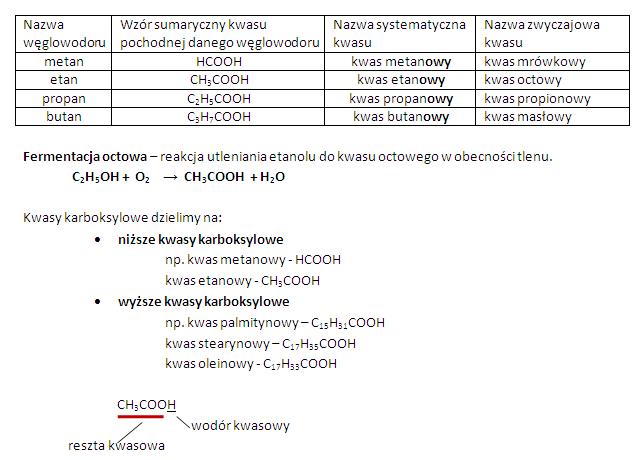
Kwasy karboksylowe otaczają nas z każdej strony. Kwas cytrynowy znajdziesz w cytrynach i innych owocach cytrusowych. Kwas mlekowy powstaje w mięśniach podczas intensywnego wysiłku i jest odpowiedzialny za zakwasy. Kwas masłowy nadaje charakterystyczny zapach zjełczałemu masłu.

Zastosowania są bardzo różnorodne. Kwas octowy wykorzystywany jest w produkcji octu i tworzyw sztucznych. Kwas benzoesowy jest konserwantem w żywności. Wyższe kwasy karboksylowe, takie jak kwas stearynowy, służą do produkcji mydeł i kosmetyków. Widzisz, jak są wszechstronne?
Mam nadzieję, że teraz kwasy karboksylowe wydają Ci się mniej straszne. Pamiętaj, chemia to przede wszystkim zrozumienie, a nie tylko wkuwanie definicji. Powodzenia na sprawdzianie!





