Sprawdzian Wiązania Chemiczne Gimnazjum Nowa Era

Wiązania chemiczne to siły, które utrzymują atomy razem, tworząc cząsteczki i związki chemiczne. Dzięki nim atomy łączą się, aby osiągnąć bardziej stabilną konfigurację elektronową.
Istnieją różne rodzaje wiązań chemicznych. Najważniejsze z nich to:
- Wiązanie jonowe: Powstaje, gdy jeden atom oddaje elektron innemu atomowi. Powstają jony (naładowane cząstki). Przykład: chlorek sodu (NaCl), czyli sól kuchenna. Sód (Na) oddaje elektron chlorowi (Cl).
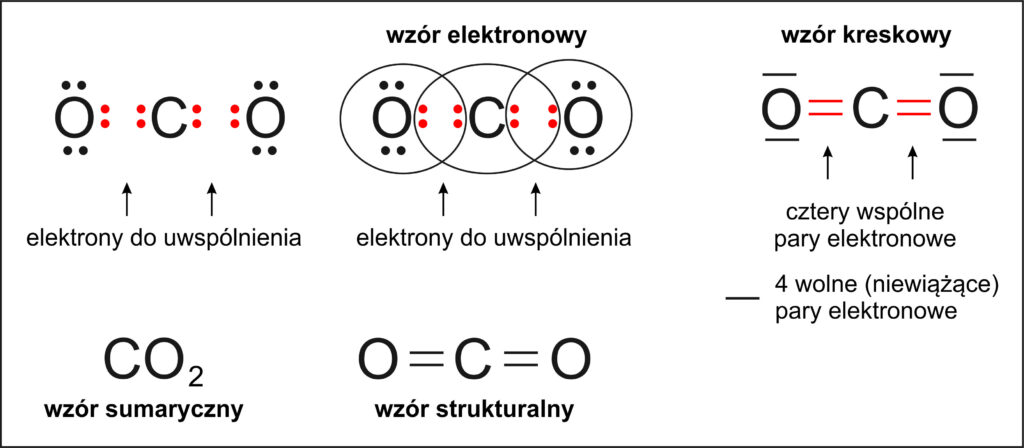
- Wiązanie kowalencyjne: Powstaje, gdy atomy wspólnie użytkowują elektrony. Jest to najczęstszy typ wiązania. Przykład: woda (H2O). Atom tlenu (O) dzieli elektrony z dwoma atomami wodoru (H). Istnieją wiązania kowalencyjne spolaryzowane i niespolaryzowane – zależnie od tego, czy elektrony są równomiernie rozdzielone.
- Wiązanie metaliczne: Występuje w metalach. Atomy metalu oddają elektrony, tworząc "morze elektronowe", które utrzymuje je razem. Dzięki temu metale dobrze przewodzą prąd.
Elektroujemność to miara zdolności atomu do przyciągania elektronów w wiązaniu. Różnica elektroujemności między atomami pozwala przewidzieć rodzaj wiązania.
Must Read
Sprawdzian z wiązań chemicznych w gimnazjum Nowej Ery zazwyczaj obejmuje rozpoznawanie rodzajów wiązań, określanie elektroujemności pierwiastków oraz przewidywanie właściwości związków na podstawie rodzaju wiązań. Zrozumienie, jak atomy łączą się, jest kluczowe dla zrozumienia chemii.
Pamiętaj! Ćwicz rozwiązywanie zadań i analizowanie różnych przykładów związków chemicznych. Powodzenia na sprawdzianie!






![Chemia klasa 7 [Lekcja 20 - Wiązanie kowalencyjne] - YouTube](https://i.ytimg.com/vi/QTtMi8VT8-s/maxresdefault.jpg)